Wojciech Rypniewski
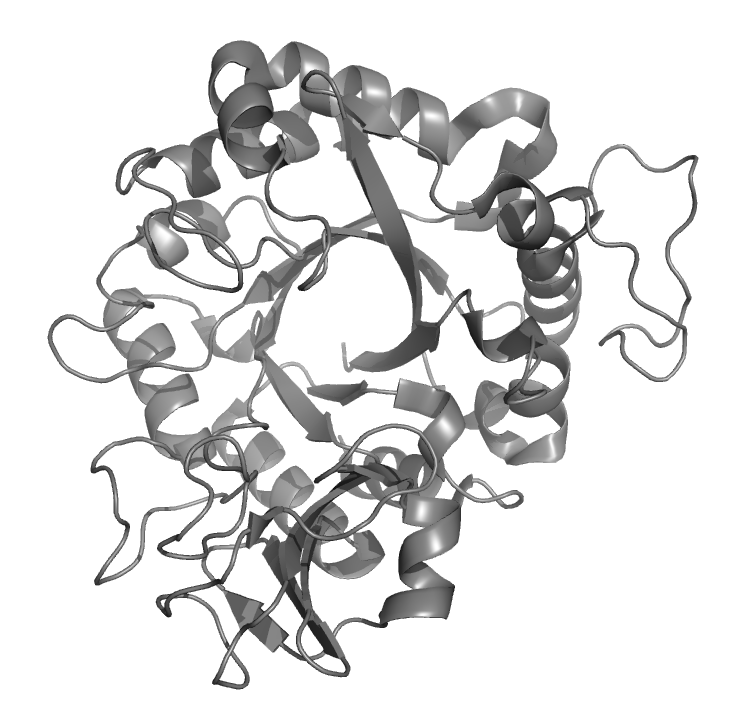
Chitynaza z termofilnej bakterii (Streptomyces thermoviolaceus). Łańcuch polipeptydowy przedstawiony jest jako wstęga. Opis białka w treści artykułu.
Białka są polimerami aminokwasów ułożonych w sekwencje charakterystyczne dla danego białka. W naturze występuje dwadzieścia różnych aminokwasów, zatem sekwencje aminokwasowe z reguły są bardzo różnorodne. Długości łańcuchów aminokwasowych (polipeptydowych) też są bardzo różne; najmniejsze białka składają się z mniej niż stu reszt aminokwasowych, a największe mają ich wiele tysięcy. Sekwencje białek zakodowane są w genach i gdy organizm potrzebuje jakiegoś białka, syntetyzuje jego łańcuch polipeptydowy według odpowiedniej sekwencji genetycznej. Analiza chemiczna pozwala ustalić sekwencje aminokwasową i długość tego łańcucha, jednak niewiele nam mówi o właściwościach i funkcji cząsteczki, bowiem natura białka zależy przede wszystkim od tego, jak ów łańcuch układa się w przestrzeni. Każde białko zwija się na swój sposób, zwykle tworząc ciasny kłębuszek albo bardziej złożoną strukturę i dopiero wówczas ujawniają się jego właściwości. Cząsteczka białka może utworzyć kształt pasujący do innego elementu w komórce i wówczas powstaje większy kompleks, który może pełnić funkcje strukturalne albo partycypować w jakimś procesie komórkowym. Często na powierzchni białka lub we wnęce na jego powierzchni zachodzą określone reakcje chemiczne. Mamy wówczas do czynienia z enzymem, czyli biologicznym katalizatorem. Miejsca, gdzie zachodzą reakcje katalityczne, zwykle są ukształtowane bardzo specyficznie, tak że spośród tysięcy różnorodnych cząsteczek znajdujących się w otoczeniu wiąże się tam tylko jeden specyficzny substrat, który następnie ulega określonej reakcji. Dzięki specyficzności reakcji enzymatycznych w komórce mogą zachodzić jednocześnie tysiące różnych procesów.
Ludzki genom koduje około dwudziestu tysięcy różnych białek. Bakterie zwykle posiadają ich kilka tysięcy, zaś genom wirusa z reguły koduje tylko kilka białek. Jeżeli weźmiemy pod uwagę różnorodność organizmów na Ziemi, mamy w sumie miliony różnych białek. Jednak wiele z nich jest między sobą spokrewnionych. Na przykład trypsyna, enzym trawienny produkowany przez trzustkę, ma bliskich krewnych w ludzkim organizmie i ma też dalszych krewnych w organizmach innych gatunków. W bakteriach też można znaleźć trypsyny o sekwencjach ewidentnie podobnych do trypsyny człowieka. Międzygatunkowe pokrewieństwo białek jest jednym z dowodów, że życie na Ziemi, choć dziś bardzo różnorodne, wyewoluowało z praorganizmu, który jest wspólnym przodkiem wszystkiego, co żyje.
Gdy mówimy o różnorodności życia na Ziemi, na myśl przychodzi przede wszystkim zróżnicowanie form i złożoności organizmów. Na tych aspektach skupiają się przyrodnicy, którzy przez popularne media przedstawiają nam szczególnie spektakularne i zadziwiające okazy zwierząt i roślin, a także nie mniej zadziwiający świat mikroorganizmów. Dla biologa jeszcze bardziej zdumiewające są zdolności organizmów do zasiedlania różnorodnych środowisk, w których panują warunki wręcz ekstremalne. Życie można znaleźć „praktycznie wszędzie”. Nie tylko na ziemi i na dnie oceanu, ale nawet w osadach kilometr pod dnem. Nawet kilka kilometrów w głąb skał tworzących skorupę ziemską, w lodzie Antarktydy i w jeziorze od tysięcy lat przykrytym lodowcem kilometrowej grubości. W alkalicznych jeziorach i kwaśnych źródłach wulkanicznych, w kominach hydrotermalnych, gdzie temperatury przekraczają 100 stopni Celsjusza, ciśnienie przekracza tysiąc atmosfer i panuje całkowita ciemność. Istnieją tam całe ekosystemy mikrobów i bardziej złożonych organizmów.
Co pozwala niektórym organizmom żyć w warunkach, które dla innych są zabójcze? Czy są inaczej skonstruowane? Czy są wyposażone w specjalne składniki, pozwalające im przetrwać, których inne organizmy nie mają? Zdarza się, że tak jest. Na przykład rośliny i zwierzęta żyjące w niskich temperaturach mogą mieć przeciwzamarzaniowe domieszki w swoich tkankach. Na ogół jednak nie znajdujemy w organizmach ekstremofilnych niczego unikalnego, co by tłumaczyło ich nadzwyczajną odporność na ekstremalne warunki. Białka są z reguły dość wrażliwe na temperaturę i łatwo ulegają denaturacji – „ścinają się”. Skala w termometrach medycznych kończy się na 42°C, bo jest to temperatura dla nas zabójcza. To znaczy, że przynajmniej niektóre białka budujące nasz organizm ulegają w tej temperaturze nieodwracalnym uszkodzeniom. Natomiast białka niektórych organizmów termofilnych są stabilne we wrzątku. Jeżeli porównamy je z naszymi białkami, nie zauważymy oczywistych różnic. Owszem, będą różnice w sekwencjach aminokwasowych, ale zwykle tak jest, gdy porównujemy białka różnych gatunków. Poza tym nie znajdziemy w termostabilnych białkach żadnych unikalnych składników, tylko te same dwadzieścia różnych aminokwasów, jak we wszystkich innych białkach.
Na drugim biegunie skali temperaturowej mamy organizmy zimnolubne (psychrofilne). Nie chodzi o samą zdolność, jaką posiada wiele roślin, do przetrwania zimy, aby wznowić wegetację, gdy się ociepli. Chodzi raczej o organizmy, które permanentnie żyją w niskich temperaturach i są do takich warunków dostosowane najlepiej. Warto zauważyć, że niskie temperatury panują w większości biosfery. Zimno jest nie tylko w obszarach okołobiegunowych, ale także w głębi oceanów, gdzie permanentnie panują temperatury bliskie zera stopni Celsjusza. Wyzwaniem dla organizmów zimnolubnych jest to, że w niskich temperaturach procesy fizykochemiczne zachodzą o wiele wolniej niż w temperaturach, które określamy jako umiarkowane. Z grubsza, spadek temperatury o każde dziesięć stopni powoduje spowolnienie reakcji chemicznych, a zatem procesów życiowych, o połowę. Dlatego żywność w lodówce psuje się kilkakrotnie wolniej niż w temperaturze pokojowej. Mimo niskich temperatur organizmy zimnolubne zachowują dość dużą żywotność, a ich enzymy mogą pracować w tempie zbliżonym do pokrewnych enzymów w organizmach żyjących w temperaturach umiarkowanych. Lodówka nie byłaby dobrym zabezpieczeniem żywności, gdyby zagnieździły się w niej psychrofile. I znów, jeżeli przyjrzymy się białkom psychrofilnym, na pierwszy rzut oka nie zauważymy niczego szczególnego, tylko kombinacje tych samych dwudziestu aminokwasów połączonych w swoiste sekwencje.
Z powyższego widać, że zrozumienie, jak można z takich samych składników budować białka o bardzo różnych właściwościach, nie jest łatwe i wymaga wnikliwej analizy. Będziemy do tego potrzebowali wiedzy o strukturze tych cząsteczek, bo jak zauważyliśmy wyżej, sama chemiczna analiza nie wystarcza, aby zrozumieć ich właściwości. Wskazane jest też, aby porównywane białka nie różniły się pod wieloma różnymi względami, bo wtedy nie będzie wiadomo, czemu przypisywać różnice między nimi. Idealnie byłoby porównywać białka podobne do siebie pod każdym względem, oprócz tego, że jedno jest odporne na wysoką temperaturę, a drugie funkcjonuje optymalnie w niskich temperaturach. W praktyce trudno znaleźć idealne przykłady, ale można porównać spokrewnione enzymy, katalizujące podobne reakcje w organizmach termofilnych i psychrofilnych. Mamy wtedy szanse, że przynajmniej niektóre z różnic między nimi będą skutkiem dostosowania do różnych temperatur.
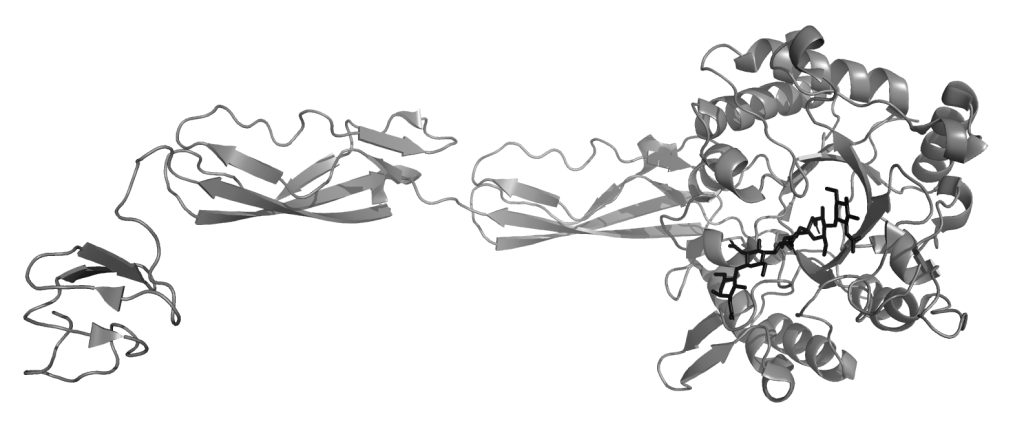
„Wstęgowy” schemat chitynazy z zimnolubnej bakterii (Moritella marina). Domena katalityczna przedstawiona jest po prawej stronie ilustracji, specjalna domena wiążąca chitynę po lewej. Fragment chityny, składający się z pięciu połączonych reszt N-acetyloglukozaminy, związany na powierzchni enzymu, w miejscu wiązania substratu, jest przedstawiony jako czarne patyczki. Opis enzymu w treści artykułu.
Takie białka rzeczywiście istnieją. Jako przykład weźmy dość powszechne w świecie mikrobów enzymy chitynolityczne, czyli degradujące chitynę. Chityna jest drugim, po celulozie, najpowszechniejszym biopolimerem. Podczas gdy celuloza występuje głównie na lądzie, najwięcej chityny jest w morzach i oceanach. Roczną produkcję chityny przez różne organizmy szacuje się na miliard ton. Syntetyzują ją głównie grzyby, skorupiaki i owady, a w mniejszym stopniu mięczaki, niektóre ryby i płazy. Chityna i celuloza są do siebie podobne o tyle, że celuloza jest polimerem glukozy, a chityna jest polimerem związku, który jest pochodną glukozy, zawierającą dodatkowo grupę N-acetylową. Dla organizmów, które potrafią utylizować chitynę, jest ona bogatszym źródłem makroelementów niż glukoza, gdyż oprócz atomów węgla i tlenu zawiera też biologicznie cenny azot. Jednak w porównaniu z celulozą chityna jest w znikomym stopniu wykorzystywana przez człowieka. Jest utylizowana głównie przez mikroorganizmy, które degradują większość szczątków organicznych w morzach i oceanach, nawet zanim opadną one na dno.
Trawienie chityny zaczyna się od cięcia polimeru na krótkie oligomery, które następnie są dalej docinane, a produktem końcowym mogą być łatwo przyswajalna przez organizm glukoza albo glukozamina. Enzymem, który zaczyna proces trawienia chityny, jest chitynaza. Chitynazy można podzielić na kilka spokrewnionych rodzin. Każdą rodzinę tworzą enzymy podobne na poziomie sekwencji aminokwasowej, co świadczy o ich pokrewieństwie. To znaczy, że geny kodujące te chityny prawdopodobnie wyewoluowały z jednego „pragenu” hipotetycznej „prachitynazy”, który jest wspólnym przodkiem znanych nam dzisiaj chitynaz. Przykład ten pokazuje, że ewolucję można obserwować nie tylko na poziomie organizmów czy całych genomów, ale też na poziomie indywidualnych genów. Analizując podobieństwa i różnice pokrewnych genów z różnych organizmów, możemy układać drzewa filogenetyczne obrazujące ich pokrewieństwo. Drzewa filogenetyczne dla poszczególnych genów często podobne są do drzew filogenetycznych dla całych gatunków.
Porównajmy zatem pokrewne chitynazy z organizmów dostosowanych do odmiennych temperatur. Chitynazę z termofilnej bakterii Streptomyces thermoviolaceus można znaleźć w fermentującym kompoście. Organizm ten musi być odporny na wysoką temperaturę otoczenia, którą w dużym stopniu sam generuje swoją aktywnością. Struktura tej chitynazy posiada cechy, które można znaleźć także w innych białkach termofilnych. Białko to jest stosunkowo niewielkie w porównaniu na przykład z chitynazą bakterii zimnolubnej Moritella marina, który żyje w zimnych głębinach oceanu. Łańcuch polipeptydowy termostabilnego enzymu tworzy zwarty kłębuszek, a pętle, jakie ten łańcuch tworzy na powierzchni cząsteczki, są stosunkowo krótkie. Obrazowo mówiąc, cząsteczka ta ma zminimalizowaną liczbę słabych punktów, od których mogłoby zacząć się luzowanie i rozplatanie struktury. Integralność cząsteczki dodatkowo wzmacniają wiązania disiarczkowe, które spinają łańcuch polipeptydowy w kilku punktach, stabilizując jego natywną konformację. Wiązań disiarczkowych jest statystycznie więcej w białkach termostabilnych niż w innych porównywalnych białkach. Więcej jest też wiązań typu mostki solne, czyli wiązań wodorowych, które są dodatkowo wzmocnione oddziaływaniami elektrostatycznymi. Powyższe cechy, a także inne, niewymienione tu, można znaleźć dość często w białkach termostabilnych, ale występują one też w innych białkach. Może też być tak, że w jakimś białku termostabilnym akurat nie znajdujemy którejś z nich. Można powiedzieć, że powyższe cechy wskazują na termostabilność, ale nie determinują jej jednoznacznie. Wyłania się obraz dość typowy dla biologii, że reguły są, ale dość ogólne i z licznymi odstępstwami. W przypadku termostabilności wydaje się, że można ją osiągnąć na różne sposoby i dla każdego białka może to być inny miks.
Oprócz samej stabilności strukturalnej białka ważne jest to, żeby ono dobrze funkcjonowało jako enzym w wysokiej temperaturze. Problemem może być to, że w wysokiej temperaturze wszystkie cząsteczki, także te, które są celem enzymów, mają dużo energii kinetycznej. Energicznie się ze sobą zderzają i równie łatwo oddalają od siebie. Aby zaszła właściwa reakcja między substratem a enzymem, muszą się one znaleźć w specyficznym i stabilnym kontakcie dostatecznie długo. W termostabilnej chitynazie miejsce wiązania substratu ma kształt dość głębokiej bruzdy na powierzchni enzymu. Ułatwia to specyficzne wiązanie i zwiększa szanse, że dojdzie do właściwej reakcji zanim substrat się oddali. Inaczej to wygląda w przypadku chitynazy zimnolubnej bakterii Moritella marina. W niskich temperaturach cząsteczki są mniej mobilne, a zatem mniejsza jest szansa, że w ogóle dojdzie do produktywnego kontaktu i reakcji enzymu z substratem. Być może dlatego w zimnolubnej chitynazie miejsce wiązania substratu jest płytkie i zoptymalizowane pod kątem „przystępności” enzymu dla substratu i gotowości do reakcji z nim. Płytkie oddziaływanie ma tę zaletę, że łatwiej do niego dochodzi i tę wadę, że jest mniej specyficzne i może być nieproduktywne, czyli może nie dojść do reakcji. Jak ten problem jest rozwiązany w przypadku zimnolubnego enzymu? Chitynaza z bakterii Moritella marina posiada kilka cech, które mogą wspomagać jej funkcjonowanie w niekorzystnych warunkach temperaturowych. Jest cząsteczką znacznie większą i bardziej złożoną od opisanego wyżej termofilnego białka, i może wiązać substrat w niejednym miejscu i na kilka sposobów, co kompensuje problem ze słabszym wiązaniem w miejscu, gdzie bezpośrednio zachodzi kataliza. Enzym ma kształt wydłużony i składa się z czterech domen połączonych elastycznymi przegubami. Z jednej strony znajduje się domena katalityczna, a na drugim końcu jest mała domena, która mocno wiąże chitynę. Możemy sobie wyobrazić, że tą domeną białko mocno przylega do rozległej powierzchni chityny, a domena katalityczna, na drugim końcu cząsteczki, „rozdziobuje” powierzchnię chityny znajdującą się w jej zasięgu, rozrywając wiązania tworzące ten polimer. Ponadto, mimo że miejsce wiązania substratu na domenie katalitycznej jest płytkie, to na jego przedłużeniu znajduje się element przypominający mobilną wypustkę, której rolą prawdopodobnie jest poluzowanie zwartej struktury chityny, aby łatwiej ją było rozcinać.
Takie obserwacje budzą pewien optymizm, że może zaczynamy rozumieć reguły determinujące stabilność białek i ich wydajność enzymatyczną. Jednak, aby się przekonać, czy naprawdę coś zrozumieliśmy, powinniśmy to sprawdzić doświadczalnie. Inżynieria genetyczna pozwala badaczom produkować białka modyfikowane dowolnie według życzeń badacza. Można zatem zmieniać w strukturze białka te elementy, które wydają się istotne i obserwować czy właściwości białka zmienią się zgodnie z oczekiwaniami. Na przykład, czy można zbudować białko, które łączyłoby najlepsze cechy różnych ekstremofilnych białek, byłoby termostabilne i jednocześnie wydajne enzymatycznie, jak białka zimnolubne? Elementy struktury, które nadają białku te różne właściwości, niekoniecznie nakładają się na siebie w strukturze białka. Zatem czy można by je połączyć w syntetycznym białku? Byłaby to kombinacja niewystępująca w naturze, ale mogłaby być pożyteczna dla człowieka, na przykład w przemysłowej obróbce biomateriałów.
Nie jest to łatwe, gdyż białka są bardzo delikatnie zbalansowanymi strukturami, jak domki z kart, i ingerencja w ich natywną strukturę zamiast spodziewanego efektu najczęściej skutkuje zmianami na niekorzyść. Zazwyczaj, gdy mamy do czynienia z delikatnym, skomplikowanym mechanizmem, najłatwiej jest coś zepsuć. Zamiast enzymu na życzenie, można otrzymać cząsteczkę niestabilną, nierozpuszczalną, nienadającą się do pomiarów. Jednak niektóre enzymy, wydają się bardziej obiecującymi obiektami badań, ze względu na ich „modułową” strukturę. Opisana wyżej chitynaza z zimnolubnej bakterii składa się z czterech domen połączonych w łańcuszek. Jest prawdopodobne, że łatwiej manipulować takim białkiem, na przykład usuwając pojedyncze domeny bądź układając je w inny sposób, i jest szansa, że nie wpłynie to na stabilność pozostałych domen. Rzeczywiście poszczególne domeny, zwłaszcza te większe, zachowują się tak, jakby posiadały sporą niezależność. Jednak w biologii nic nie jest proste i nawet kiedy się wydaje, że potrafimy przewidzieć skutek jakiejś manipulacji, może się okazać, że wynik jest inny od spodziewanego. „Zabawa w lego”, w której klockami są domeny białka, pokazała, że pewne kombinacje są możliwe, a inne trudniejsze do uzyskania i czasem trudno powiedzieć dlaczego. Wydaje się, że niektóre domeny ulegają destabilizacji w bliskiej obecności innych domen. Czasem też sztuczne konstrukty łatwiej ulegają degradacji niż natywne białko.
Warto też odnotować, że wbrew naiwnym oczekiwaniom, białka termostabilne nie są po prostu stabilniejszą wersją swych nietermostabilnych odpowiedników i mogą się okazać nieprzydatne w warunkach innych niż w swoim ekstremalnym środowisku. Kiedy są produkowane w temperaturze pokojowej, mogą być nieaktywne bądź aktywne w niepełnym stopniu. Czasem można je aktywować stosując „wyżarzanie” (ang. annealing) czyli podgrzewanie i inkubowanie w wyższej temperaturze. Po takiej procedurze mogą zachować aktywność nawet po ostudzeniu do temperatury pokojowej. Oznacza to, że białko potrzebowało wysokiej temperatury, aby poprawnie się sfałdować, czyli osiągnąć swą natywną strukturę. Z kolei enzymy zimnolubne, wykazujące nadzwyczaj wysoki poziom aktywności w niskich temperaturach, dość łatwo tracą aktywność nawet w temperaturze pokojowej.
Badając białka termostabilne, zgłębiamy zasady stabilności białek, a badając enzymy zimnolubne, dowiadujemy się, co czyni enzym wydajnym, jednak niełatwo jest tę wiedzę zastosować w praktyce, budując stabilne sztuczne konstrukty. Białka występujące w przyrodzie są wynikiem milionów lat niestrudzonej ewolucji i optymalizacji do funkcjonowania w bardzo konkretnych warunkach. Jednocześnie pozostają strukturami bardzo złożonymi i delikatnymi, które łatwiej zepsuć niż poprawić. Oczywiście potrafimy modyfikować białka do konkretnych celów, potrafimy nawet modyfikować całe organizmy. Jest na to wiele przykładów. Jednak czy możemy tworzyć coś „lepszego” niż to, co występuje w naturze? Czy możemy zaprojektować „superbiałka” łączące najlepsze cechy różnych naturalnych białek?
We wczesnych latach inżynierii genetycznej obawiano się, że modyfikując drobnoustroje, człowiek nieopatrznie stworzy groźną superbakterię. W praktyce okazało się, że modyfikowane przez nas organizmy z reguły są słabsze od ich dzikich kuzynów, a sterylne warunki pracy laboratoryjnej służą głównie ochronie hodowli modyfikowanych bakterii przed inwazją naturalnych drobnoustrojów. Prawdziwymi superbakteriami okazały się szczepy naturalne, optymalizowane przez miliony lat ewolucji w warunkach presji środowiska. Na razie ślepa, ale wytrwała naturalna optymalizacja metodą prób i błędów wygrywa z naszymi wciąż naiwnymi próbami projektowania.
Część opisanych badań była finansowana przez Narodowe Centrum Nauki (UMO-2017/27/B/NZ1/02201).
Prof. dr hab. Wojciech Rypniewski, Instytut Chemii Bioorganicznej PAN