Aleksander Czogalla
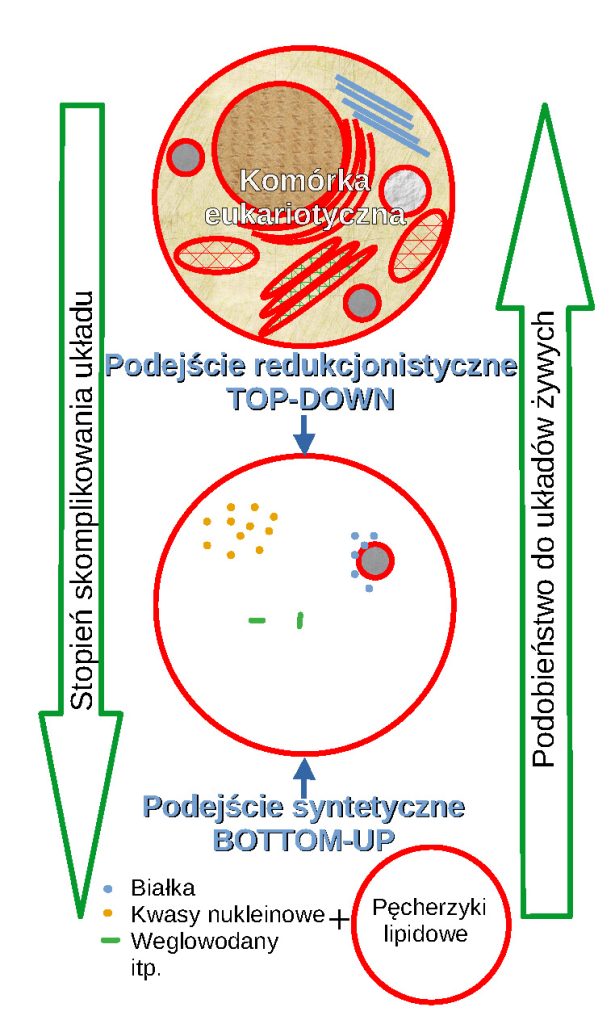
Rycina 1. Schematyczne przedstawienie głównych podejść eksperymentalnych stosowanych w biologii syntetycznej.
Rozwikłanie wszystkich tajemnic życia wciąż pozostaje poza zasięgiem naszych możliwości poznawczych. Mając do dyspozycji ograniczony zasób dalekich od doskonałości metod badawczych, nie potrafimy zbudować jednoznacznego obrazu wszystkich procesów fizjologicznych w kontekście całych komórek. A to dlatego, że poziom złożoności tych podstawowych jednostek życia utrudnia, a czasem wręcz uniemożliwia uchwycenie wszystkich szczegółów niezbędnych do poznania molekularnych mechanizmów procesów komórkowych. Na szczęście możemy korzystać z dobrodziejstw podejść opartych na biologii syntetycznej, a polegających na rekonstytucji molekuł i procesów w sztucznych systemach naśladujących układy biologiczne.
Jedna z definicji biologii syntetycznej określa ją jako racjonalne projektowanie systemów biologicznych przy wykorzystaniu technik symulacyjnych w celu jak najdokładniejszego przewidzenia zachowania się tego systemu oraz optymalizacji jego funkcjonowania. Celem nadrzędnym jest tu konstrukcja sztucznych form życia o programowalnej funkcjonalności lub posiadających zestaw cech charakterystycznych dla form żywych. Syntetyczna komórka to już jednak określenie, które nie jest jednoznacznie zdefiniowane w literaturze naukowej. A to wszystko za sprawą dwóch różnych, aczkolwiek komplementarnych względem siebie, podejść eksperymentalnych w biologii syntetycznej (Rycina 1). Jedno z nich zapoczątkowane przez J. Craiga Ventera można określić jako redukcjonistyczne (ang. top-down), a polega ono na minimalizacji naturalnego systemu (np. genomu bakterii) do poziomu wystarczającego do utrzymania podstawowych funkcji komórki. Natomiast w podejściu syntetycznym (ang. bottom-up) punktem wyjścia jest zbiór podstawowych molekuł, którego systematyczne rozszerzenie i kompilacja w określone struktury pozwalają na odtworzenie modułów funkcjonalnych. Złożoność syntetycznego układu zwiększa się krok po kroku, włączając do niego coraz więcej komponentów. Tu wychodzi się z założenia, że warunkiem pełnego poznania danego zjawiska biologicznego jest uzyskanie możliwości jego odtworzenia i kontrolowania, co jest zgodne z sensem wypowiedzi Richarda Feynmana: „What I cannot create, I do not understand”. Taką strategię z powodzeniem stosuje się obecnie do ujawnienia biologicznej roli poszczególnych składowych komórki, a narzędzia biologii syntetycznej są powszechnie wykorzystywane w laboratoriach biochemicznych i biofizycznych w celu głębszego zrozumienia reguł i współzależności na poziomie molekularnym. Podstawową cechą wszystkich komórek żywych jest ich fizyczne oddzielenie od otaczającego środowiska za pośrednictwem błony zbudowanej z dwuwarstwy lipidowej. Co więcej, komórki eukariotyczne cechuje rozbudowany system błon wewnątrzkomórkowych, którego zadaniem jest nie tylko umożliwienie przeprowadzania procesów fizjologicznych wymagających środowiska dwuwarstwy lipidowej, ale także utworzenie zamkniętych nanokompartymentów oddzielonych od cytoplazmy. Dlatego rekonstytucja procesów komórkowych bardzo często wymaga uwzględnienia komponentów lipidowych będących w stanie tworzyć struktury odpowiadające błonom komórkowym lub subkomórkowym.
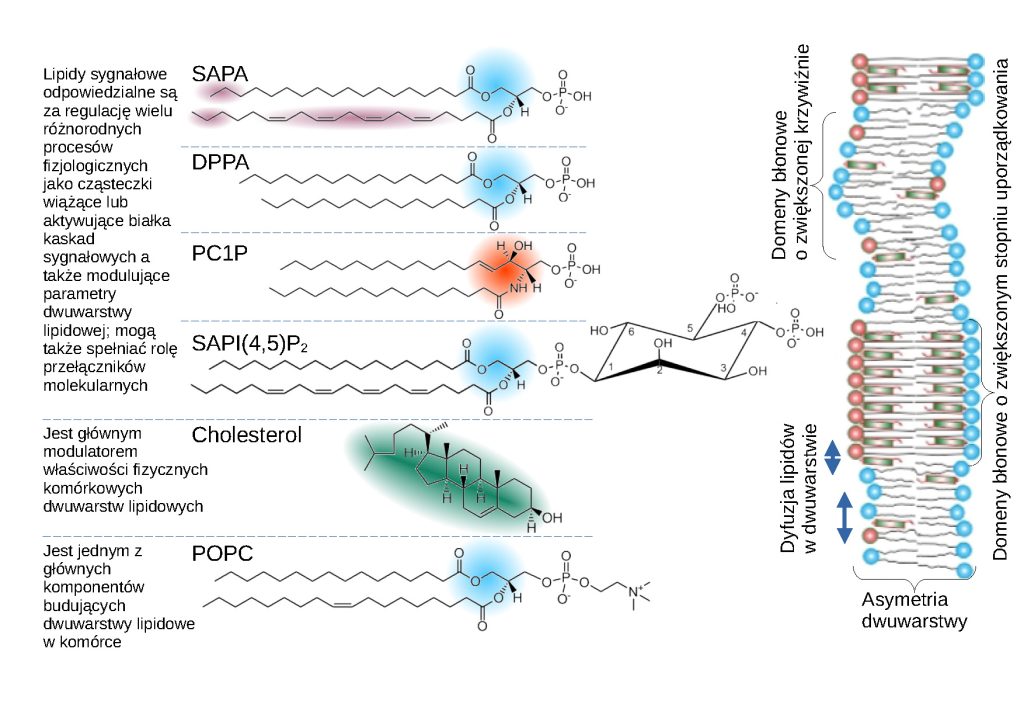
Rycina 2. Przykłady lipidów tworzących dwuwarstwy, które definiują błony komórkowe. Różnorodność lipidów błonowych związana jest z różnicami w strukturze łańcuchów acylowych (por. SAPA z DPPA, różnice zaznaczone kolorem fioletowym), obecnością charakterystycznych grup funkcyjnych (por. DPPA reprezentujący glicerofosfolipidy z PC1P reprezentującym sfingolipidy, główne różnice zaznaczone odpowiednio kolorem niebieskim i czerwonym) lub reszt funkcyjnych przyłączonych do grup fosforanowych (por. SAPA z SAPI(4,5)P2). Sterole, takie jak cholesterol, charakteryzują się odmienną strukturą wielopierścieniową. Nazwy chemiczne lipidów: SAPA – 1-stearylo-2-arachidonylo-sn-glycero-3-fosforan, DPPA – 1,2-dipalmitylo-sn-glycero-3-fosforan, PC1P – N-palmitylo-ceramido-1-fosforan, SAPI(4,5)P2 – 1-stearylo-2-arachidonylo-sn-glycero-3-fosfo-(1’-mio-inozytol-4’,5’-bisfosforan), POPC – 1-palmitylo-2-oleilo-glycero-3-fosfocholina. W błonach biologicznych lipidy różnią się od siebie sposobem zachowania się, co może objawiać się m.in. różnym tempem dyfuzji, niehomogennością rozmieszczenia w dwuwarstwach ze względu na asymetrię oraz generowaniem domen o odmiennym stopniu uporządkowania lub krzywiźnie.
Błony biologiczne są strukturami definiującymi każdą żywą komórkę. Wynika to głównie z ich właściwości barierowych, które predestynują je do pełnienia roli oddzielania wnętrza komórki od otoczenia i zapewniania odpowiedniej organizacji strukturalnej i funkcjonalnej na poziomie subkomórkowym. Jednak w ostatnich latach postrzeganie błon biologicznych i roli, jaką odgrywają budujące je lipidy, uległo radykalnej zmianie. Z pewnością przyczynił się do tego lawinowy przyrost danych lipidomicznych. Intensywne prace nad jakościową i ilościową analizą profilu lipidów w komórce pozwoliły na skatalogowanie ponad 48 tys. strukturalnie różnych cząsteczek lipidowych (por. baza danych www.lipidmaps.org), a ilość pozycji tego katalogu z pewnością w najbliższych latach znacznie się zwiększy. Po co komórce taka różnorodność? Konsternacja spowodowana tym pytaniem zniknie, jeśli uświadomimy sobie, że cząsteczki lipidów to nie tylko pasywne elementy strukturalne tworzące bariery w postaci selektywnie przepuszczalnej dwuwarstwy, ale także elementy aktywnie kształtujące wiele fizjologicznych procesów komórkowych, m.in. tych związanych z przekazywaniem sygnału (Rycina 2). Mogą one oddziaływać ze sobą w różnych konfiguracjach, tworząc przedziały (domeny) błonowe wyróżniające się m.in. sposobem uporządkowania cząsteczek lipidowych lub parametrami geometrycznymi (na przykład stopniem zakrzywienia dwuwarstwy). Co więcej, chociaż właściwości fizykochemiczne błon komórkowych w przeważającym stopniu determinowane są przez tworzące dwuwarstwę lipidy, to jednak za przebieg procesów fizjologicznych w dużej mierze odpowiadają integralne i peryferyjne białka błonowe. Do funkcjonowania tych białek niezbędne są wzajemne interakcje z lipidami (bądź domenami błonowymi) lub innymi białkami błonowymi w szerokiej skali czasowej i przestrzennej. Oddziaływanie białek z lipidami błon nie tylko determinuje lokalizację danego białka w konkretnym miejscu komórki, ale może także kontrolować jego aktywność (np. enzymatyczną). Znamienne jest, że komórki eukariotyczne poświęcają ogromną cześć swoich zasobów, rezerw energetycznych oraz czasu na generowanie ogromnej różnorodności składowych błon jak również na utrzymanie odpowiedniej organizacji tego typu struktur w kontekście czasoprzestrzennej dystrybucji cząsteczek lipidów i białek błonowych, generowanie strukturalnie i funkcjonalnie rozróżnialnych domen oraz utrzymywanie asymetrii.
Jedno z podstawowych pytań dotyczy więc zachowania specyficzności podczas rozpoznawania lipidów danego typu przez białka efektorowe. Badania tych zależności i wzajemnych interakcji na modelu komórkowym przysparzają bardzo wielu problemów natury metodologicznej, a uzyskane wyniki bardzo często uniemożliwiają wyciągnięcie jednoznacznych konkluzji. Co więcej, w przeciwieństwie do białek, których poziom w komórce można stosunkowo łatwo regulować poprzez precyzyjne narzędzia umożliwiające ingerencję na poziomie genów lub mRNA, lipidy nie poddają się tak łatwo manipulacji w sposób bezpośredni w kontekście całej komórki bądź poszczególnych organelli. Rozwiązaniem może być zastosowanie podejścia biologii syntetycznej i rekonstytucja badanych cząsteczek oraz procesów z użyciem modelowych systemów błonowych.
Dlaczego w badaniach naukowych musimy wspierać się eksperymentami z wykorzystaniem sztucznych układów błonowych jedynie naśladujących systemy biologiczne, ryzykując przy tym zbyt daleko idącym uproszczeniem układu badawczego i zwiększoną podatnością na rejestrowanie artefaktów? Przeciętny hepatocyt (podstawowy typ komórek wątroby) przy swojej objętości wynoszącej ok. 5000 µm3 zbudowany jest z błon o całkowitej powierzchni 110 000 µm2. Błony te charakteryzują się różnorodnością strukturalną lipidów je budujących, a z drugiej strony podkreślić należy mnogość białek z nimi związanych. Około 30% genów zidentyfikowanych w naszym genomie koduje integralne białka błonowe (czyli te, które na stałe są zakotwiczone w dwuwarstwie lipidowej). Co więcej, w komórce funkcjonuje ogromna ilość peryferyjnych białek błonowych, które w sposób fakultatywny oddziałują z dwuwarstwą lipidową. Znaczenie tych oddziaływań można zilustrować na przykładzie kinaz białkowych, podstawowych komponentów wewnątrzkomórkowych szlaków przekazywania sygnału, z których u ponad 10% zidentyfikowano motywy strukturalne będące miejscami wiązania lipidów. Zwykle w modelowych systemach błonowych różnorodność strukturalna lipidów jest zredukowana do kilku (rzadziej kilkunastu) różnego rodzaju cząsteczek, które konfrontuje się z uprzednio wyizolowanymi cząsteczkami białka danego typu. Wady wynikające z tak głębokiego uproszczenia układu badawczego są jednak z nawiązką kompensowane możliwościami kontrolowania warunków eksperymentalnych (nie tylko parametrów fizycznych, takich jak temperatura, ale także stosunków stechiometrycznych oddziałujących ze sobą molekuł, doboru stężeń substancji, takich jak na przykład jony wapnia, potencjalnie modulujących badane oddziaływania lub dwuwarstwę lipidową itd.). To właśnie możliwość zachowania odpowiedniej precyzji w doborze komponentów i warunków pozwala na identyfikację mechanizmów na poziomie molekularnym oraz budowanie pełnego obrazu danego zjawiska krok po kroku. Różnorodność modelowych systemów błonowych stosowanych we współczesnej praktyce badawczej wynika z jednej strony z potrzeby monitorowania konkretnych parametrów danego układu, a z drugiej strony z konieczności dostosowania układu do aparatury pomiarowej używanej w eksperymencie. Tak więc mamy do czynienia z różnego rodzaju błonami podpartymi na stałym podłożu, które może być dodatkowo modyfikowane chemicznie lub wykazywać predefiniowane cechy nieplanarnej geometrii (ang. supported lipid bilayers, SLB) albo z lipidami samoorganizującymi się na interfazie powietrze – woda. Jednak najczęściej wykorzystywane modelowe systemy błonowe opierają się na różnej wielkości pęcherzykach, co jest w dużej mierze podyktowane chęcią zbliżenia się do struktur o pokroju zbliżonym do komponentów komórkowych (Rycina 3). Zainteresowanych bardziej szczegółowym opisem modelowych systemów błonowych wraz z analizą ich potencjału w badaniach biologicznych zachęcam do zapoznania się z naszym artykułem przeglądowym (https://www.sciencedirect.com/science/article/pii/S1388198113002850?via%3Dihub).
By jak najskuteczniej zminimalizować prawdopodobieństwo wystąpienia wspomnianych już artefaktów wynikających z uproszczenia badanych systemów, niezwykle ważne jest wykorzystywanie szeregu komplementarnych względem siebie modeli błonowych. W ten sposób przynajmniej część mankamentów wynikających z natury danego systemu modelowego może zostać wyeliminowana dzięki bezpośredniemu skonfrontowaniu danych z wynikami uzyskanymi na innym modelu. Duży nacisk powinien też być położony na zastosowanie rozbudowanych eksperymentów kontrolnych, jak najdokładniejszą charakterystykę stosowanych systemów oraz ścisłą kontrolę warunków pomiarowych.
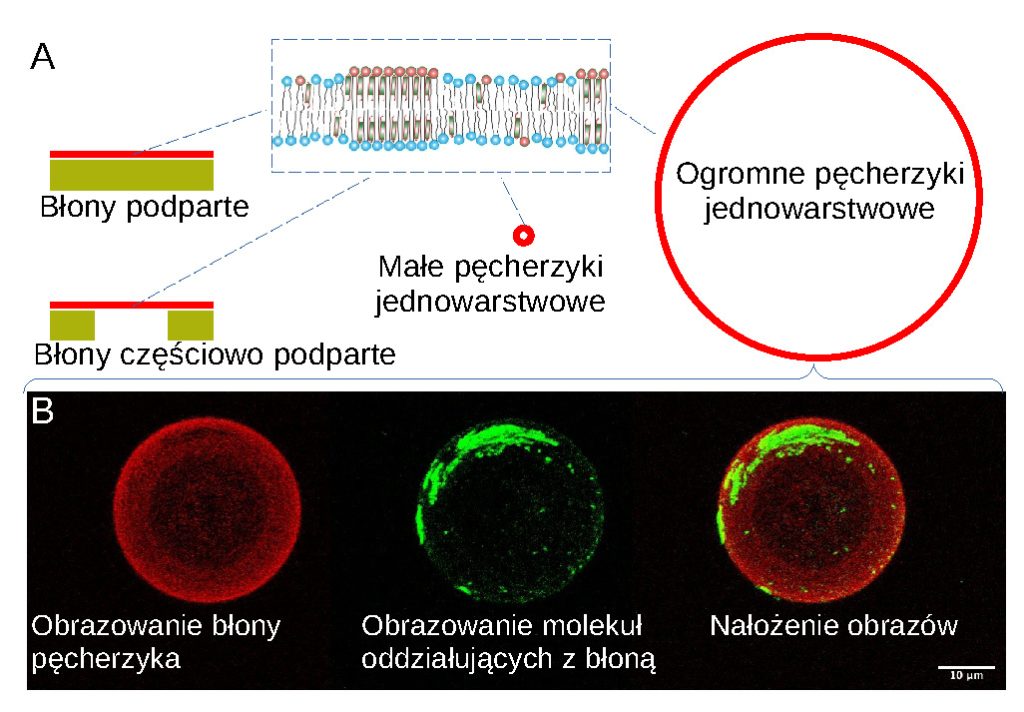
Rycina 3. Przykłady modelowych systemów błonowych powszechnie wykorzystywanych w badaniach biologicznych (A). Ogromne pęcherzyki jednowarstwowe (ang. giant unilamellar vesices, GUVs) mogą być bezpośrednio obrazowane za pomocą mikroskopii konfokalnej i rekonstrukcji trójwymiarowej (B). Błony wyznakowano amfipatycznym fluoroforem emitującym światło czerwone, cząsteczki oddziałujące z błonami i tworzące domeny na ich powierzchni wyznakowano fluoroforem emitującym światło zielone.
Mechanizmy funkcjonowania poszczególnych komponentów błon biologicznych oraz ich wzajemne oddziaływania są w ostatnich latach przedmiotem zwiększonego zainteresowania, co sprzyja także szybkiemu rozwojowi podejść metodologicznych pozwalających zgłębić te aspekty biologii komórki. Lipidy błonowe obejmują szeroką gamę cząsteczek sygnałowych (por. Rycina 2), które charakteryzują się ogromną różnorodnością pod względem zachowania się w błonie. Z pewnością w tym aspekcie wszystkie one różnią się diametralnie od cząsteczek sygnałowych funkcjonujących poza błonami (np. w cytoplazmie lub w przestrzeni międzykomórkowej). Najbardziej oczywista różnica wynika z ograniczenia dyfuzji lipidów do pseudodwuwymiarowej przestrzeni dwuwarstwy lipidowej. Z drugiej strony cząsteczki sygnałowe zakotwiczone w błonie stanowią integralną część tej błony i zanurzone są w niej niczym w pewnego rodzaju macierzy. Fakty te przemawiają za koniecznością odejścia od powszechnego do niedawna założenia, że białka (a w szczególności białka peryferyjne) oddziałują z lipidami poprzez bezwarunkowe rozpoznanie danego lipidu w dwuwarstwie i wiązanie go przy określonym stosunku stechiometrycznym i z absolutną specyficznością. W rzeczywistości trzeba brać pod uwagę fakt, że zachowanie lipidów w błonie może się zmieniać za sprawą bardzo wielu czynników, m.in. geometrii dwuwarstwy, sąsiadujących cząsteczek lipidów i białek w błonie lub cząsteczek (np. jonów) w środowisku wodnym, w którym błona się znajduje. To skłoniło mnie do zaproponowania parametru określanego jako prezentacja lipidów na interfazie błona – środowisko wodne (ang. lipid presentation) jako istotnego (poza tożsamością chemiczną/strukturalną i segregacją czasoprzestrzenną) elementu wpływającego na specyficzność oddziaływań białko – lipidy błonowe. Różnice w prezentacji danego typu lipidu skutkować mogą m.in. koegzystencją w komórce, a nawet w danej strukturze błonowej, funkcjonalnie odmiennych subpopulacji lipidów danego typu różniących się zdolnością do wiązania docelowych białek.
W naszym laboratorium prowadzimy intensywne prace nad rozwikłaniem zagadki modulacji tej specyficzności poprzez subtelne różnice strukturalne poszczególnych lipidów a także lokalne fluktuacje parametrów fizykochemicznych dotyczących zarówno błony, w której takie lipidy sygnałowe się znajdują, jak i środowiska w bezpośrednim sąsiedztwie tej błony. Wraz z zespołem koncentrujemy uwagę na słabo dotychczas poznanych regułach rządzących specyficznością oddziaływania białek z lipidami sygnałowymi, m.in. kwasem fosfatydowym (PA) i ceramido-1-fosforanem (C1P) (por. Rycina 2). Są to dość nietypowe lipidy błonowe ze względu na ich stożkowy kształt molekularny, co wiąże się z ich tendencją do zaburzania struktur dwuwarstwowych charakterystycznych dla błon biologicznych oraz generowania zakrzywień i odkształceń. Drugą charakterystyczną cechą obu lipidów jest negatywny ładunek wypadkowy ich cząsteczek oraz to, że jego wartość jest zależna od pH w fizjologicznym zakresie. Ten fakt wskazuje na to, że oba lipidy mogą odgrywać rolę molekularnych przełączników wrażliwych na chwilowe i lokalne zmiany wewnątrzkomórkowego pH, gdyż wraz ze wzrostem ładunku wypadkowego wzrasta siła oddziaływań jonowych tworzonych z partnerami białkowymi. Ze względu na podobieństwa strukturalne należałoby się spodziewać dużego stopnia konwergencji funkcjonalnej obu lipidów, jednak w rzeczywistości mamy do czynienia z zupełnie odwrotną sytuacją, gdyż każdy z wymienionych lipidów odgrywa inną rolę w komórce, a w niektórych przypadkach mogą nawet być funkcjonalnymi antagonistami. Co więcej, mnogość procesów komórkowych, w których lipidy te są zaangażowane, sugeruje, że muszą istnieć mechanizmy molekularne pozwalające na precyzyjną i wielopoziomową kontrolę ich aktywności. Nasze poszukiwania molekularnych podstaw tych mechanizmów oparliśmy na podejściach eksperymentalnych wywodzących się z biologii syntetycznej. Wyniki uzyskane dzięki zastosowaniu modelowych systemów błonowych, takich jak monowarstwy lipidowe na granicy faz woda – powietrze oraz pęcherzyki lipidowe o różnej średnicy w badaniach in vitro konfrontowaliśmy z rezultatami naszych szeroko zakrojonych badań in silico obejmujących m.in. symulacje dynamiki molekularnej oraz modelowania Monte Carlo. W ten sposób zidentyfikowaliśmy kilka działających niezależnie od siebie mechanizmów regulacji aktywności lipidów.
Jeden z wątków dotyczy białka mTOR, wielodomenowej kinazy białkowej, która jest kluczowym regulatorem metabolizmu, wzrostu, proliferacji i ruchu komórki. Wcześniejsze badania na modelu komórkowym wskazywały, że PA działa na to białko stymulująco bądź hamująco w zależności od struktury łańcuchów acylowych tego lipidu (por. Rycina 2). Wyniki naszych badań wskazują, że ma to swoje odzwierciedlenie w zmiennej specyficzności mTOR względem różnych subpopulacji molekularnych tego lipidu (https://www.mdpi.com/2073-4409/11/1/119). Wśród specjalistów panuje przekonanie, że cząsteczki PA o nasyconych łańcuchach acylowych predystynowane są do magazynowania energii na drodze przekształcania ich w triacyloglicerole, co znajduje odzwierciedlenie w ich hamującym wpływie na mTOR, podczas gdy PA o nienasyconych łańcuchach acylowych aktywują mTOR, a tym samym sprzyjają proliferacji. Wyniki naszych badań wskazują też, że obecność cholesterolu w błonie mocno wpływa na te oddziaływania. Jest to niezwykle interesujące, jeśli weźmiemy pod uwagę, że cholesterol jest postrzegany jako główny modulator właściwości fizycznych błon komórkowych i pełni także kluczową rolę w procesach formowania domen błonowych (tzw. tratw lipidowych). Te ostatnie stanowią strukturalne i funkcjonalne platformy o zróżnicowanym znaczeniu fizjologicznym. Bardziej szczegółowe badania pozwoliły nam na stwierdzenie, że mechanizm opisywanego procesu zmiennej prezentacji cząsteczek PA polega na wzajemnych oddziaływaniach pomiędzy poszczególnymi lipidami sygnałowymi a cholesterolem (https://www.mdpi.com/1422-0067/22/21/11523). Podobne analizy pozwoliły nam opisać zachowanie i formowanie domen przez C1P w dwuwarstwach lipidowych w zależności od stopnia nasycenia łańcuchów acylowych (https://www.nature.com/articles/s41598-023-45575-5). W toku naszych badań okazało się także, że wiązanie jonów wapnia do główek polarnych lipidów sygnałowych powoduje nie tylko neutralizację ładunku wypadkowego, ale także znaczne zmiany konformacyjne ostatnich z wymienionych. Zmiany te z kolei silnie wpływają na interakcje z białkowymi składnikami kaskad sygnałowych komórki (https://pubs.acs.org/doi/10.1021/jacs.6b11760).
Nasze wyniki pozwalają na wypełnienie szeregu luk występujących w obrazie funkcjonowania komórkowych szlaków sygnałowych. Jedną z takich zagadek jest ogromna liczba zidentyfikowanych dotychczas partnerów białkowych wiążących daną klasę lipidów sygnałowych w komórkach różnych organizmów. Ta dysproporcja jest nieadekwatna do podtrzymania wymaganej kierunkowości i specyficzności poszczególnych odpowiedzi komórkowych. Teraz wiemy, że dotychczas ignorowane subtelne różnice strukturalne w łańcuchach acylowych lipidów sygnałowych znacząco zmieniają zachowanie się tych lipidów w odniesieniu do białek efektorowych, a sąsiadujące z nimi w błonie lipidy (np. cholesterol) i wtórne przekaźniki sygnału (np. jony wapnia) odgrywają tu rolę dodatkowych modulatorów. Chociaż pojawienie się danego lipidu konkretnej lokalizacji w komórce jest niezbędne do uruchomienia poszczególnych procesów sygnałowania, to jednak to, czy dany proces zostanie uruchomiony i w jaki sposób będzie przebiegał, zależy w dużym stopniu od kontekstu molekularnego, w którym prezentowany jest ten lipid. Odkrycia te niosą ze sobą bardzo istotny walor poznawczy, ale także rzucają nowe światło na metodykę identyfikacji molekuł i procesów fizjologicznych przy poszukiwaniach nowych celów terapeutycznych.
Cześć opisanych badań była finansowana przez Narodowe Centrum Nauki (projekt nr 2018/30/E/NZ1/00099) oraz Ministerstwo Nauki i Szkolnictwa Wyższego (projekt Iuventus Plus IP2014 007373) .
Dr hab. Aleksander Czogalla, prof. UWr., kierownik Zakładu Cytobiochemii, Wydział Biotechnologii Uniwersytetu Wrocławskiego