Robert Czajkowski
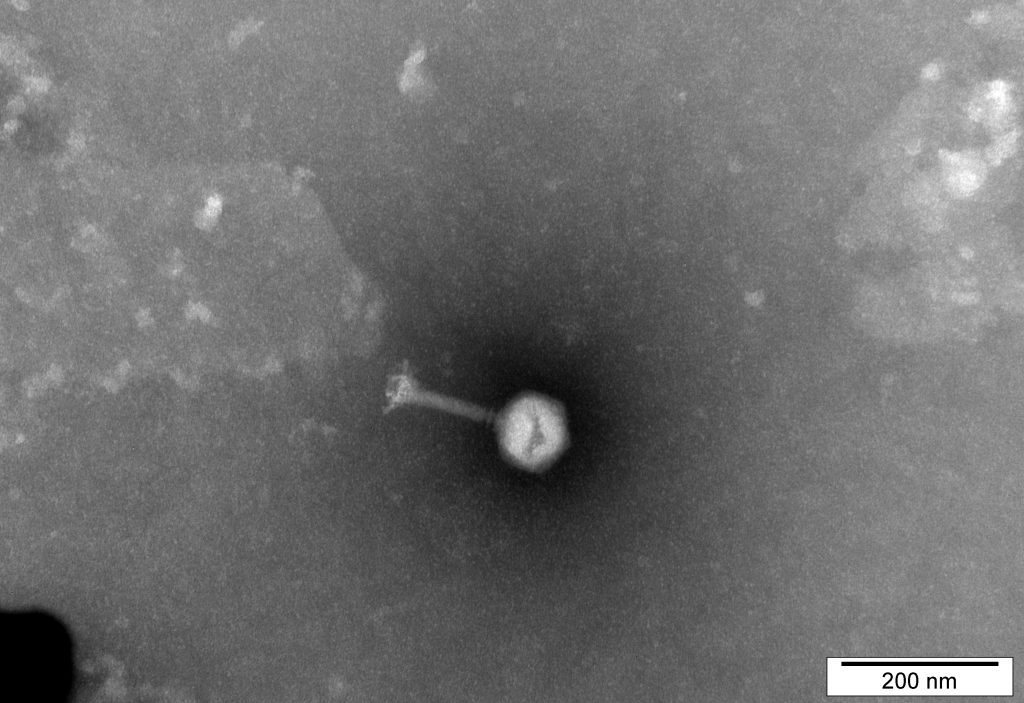
Zdjęcie bakteriofaga (wirusa bakteryjnego) z transmisyjnego mikroskopu
Bakteriofagi, znane również jako fagi, to wirusy atakujące i zabijające wyłącznie bakterie. Wraz z rozwojem badań nad tymi wirusami stało się jasne, że istnieją też takie fagi, które po zakażeniu gospodarza nie powodują jego natychmiastowej śmierci, ale wbudowują swój genom do bakteryjnego genomu i bytują w takiej formie uśpienia, nie czyniąc szkody gospodarzowi. Takie sekwencje wirusowe w genomach bakterii zostały nazwane profagami. Niesamowite jest to, że te sekwencje występują w genomach większości, jeżeli nie wszystkich bakterii, które kiedykolwiek odkryto i zbadano.
Profagi odgrywają szczególnie interesującą rolę w ewolucji i adaptacji bakterii. Mogą być (i bardzo często są!) dziedziczone przez potomne komórki. Wpływają globalnie na wygląd (fenotyp) i zachowanie bakterii oraz na zdolność do wywoływania chorób czy też przetrwania w różnych warunkach środowiskowych.
Co ciekawe, profagi mogą kodować i przenosić obce geny, dając gospodarzowi nowe cechy, takie jak np. geny kodujące czynniki wirulencji lub czynniki umożliwiające korzystną adaptację gospodarza do zasiedlanego środowiska. Aktualnie przyjmuje się powszechnie, że obecność tych sekwencji w genomach bakterii stanowi jeden z najważniejszych motorów adaptacji i ewolucji bakterii w środowisku. I tak dzieje się od setek tysięcy lat.
Profagi mogą być postrzegane nie tylko jako wirusy bakteryjne, ale także jako cisi „współpracownicy” bakterii. Na przykład mogą chronić swoich bakteryjnych gospodarzy przed infekcją innymi wirusami. Dzięki temu bakterie, które posiadają w swoim genomie profagi, łatwiej przeżywają i mogą lepiej konkurować z innymi bakteriami w środowisku.
A gdyby tak wykorzystać profagi do zmiany wyglądu i zachowania komórki bakterii? Gdyby zaprojektować sztuczne sekwencje wirusowe, wprowadzać je do genomu bakterii i w ten sposób sterować i zmieniać metabolizm bakterii oraz ich adaptację i ewolucję? A gdyby wykorzystać do tego najnowsze zdobycze biologii syntetycznej?
No właśnie, biologia syntetyczna, czyli nowa i ekscytująca dziedzina nauki, która stanowi podstawę innowacyjnych projektów biotechnologicznych a także projektów pozwalających zmieniać świat. Czym zatem jest?
Biologia syntetyczna to jedna z najnowocześniejszych dziedzin nauki. Łączy w sobie elementy biologii, inżynierii, informatyki, chemii oraz technologii. Wszystko po to, by projektować i budować „nowe formy życia” lub modyfikować te istniejące w naturze (np. wspomniane bakterie) w precyzyjny i celowany sposób. Celem biologii syntetycznej jest stworzenie nawet całych syntetycznych komórek, które mogą spełniać konkretne funkcje, takie jak produkcja leków, biopaliw, czy wykrywanie zanieczyszczeń środowiskowych.
W praktyce, w dużym skrócie, biologia syntetyczna polega na manipulowaniu kwasem nukleinowym (DNA), molekularnym „kodem życia”. Naukowcy mogą projektować nowe sekwencje genów, wykorzystując do tego specjalistyczne programy komputerowe, a następnie syntetyzować je w laboratorium. Te syntetyczne geny są następnie wprowadzane do komórek, gdzie zaczynają działać. I tutaj rozpoczyna się magia. Dzięki biologii syntetycznej możliwe jest np. stworzenie bakterii, które produkują substancje chemiczne potrzebne do tworzenia leków, lub roślin, które są bardziej odporne na zmiany klimatyczne.

Bakteriofagi wydrukowane na drukarce 3D, przygotowane przez studentów iGEM 2023 – IFB Gdańsk Team
W erze biologii syntetycznej profagi zyskują nowe znaczenie: stają się niezwykle użytecznymi narzędziami, które mogą być wykorzystane do projektowania syntetycznych genomów bakterii a także do tworzenia syntetycznych bakteriofagów mających na celu kontrolę różnych patogennych bakterii w środowisku.
Syntetyczne bakteriofagi to zatem wirusy bakteryjne zaprojektowane całkowicie przy użyciu technik inżynierii genetycznej, które mogą być modyfikowane w celu zwiększenia ich skuteczności, specyficzności i bezpieczeństwa. Dzięki możliwościom, jakie daje biologia syntetyczna, możliwe jest tworzenie fagów, które są odporne na zmiany środowiskowe, mają zdolność do celowania w konkretne szczepy bakterii, a także mogą przenosić geny kodujące dodatkowe białka lub enzymy, które wspomagają walkę z infekcjami. W ramach projektowania syntetycznych genomów profagi mogą być wykorzystane do wprowadzenia do bakterii genów zwiększających ich zdolność do przetrwania i konkurencji w różnych warunkach środowiskowych.
Właśnie wykorzystanie biologii syntetycznej do modyfikacji sekwencji wirusowych obecnych w bakteriach i zaprojektowanie syntetycznych genomów bakteriofagów zaplanowałem w swoim projekcie Sonata Bis 10 (2020/38/E/NZ9/00007) finansowanym przez Narodowe Centrum Nauki. Na badania w ramach tego pięcioletniego projektu otrzymałem ponad 3 miliony złotych.
Sonata Bis to prestiżowe konkursy na badania naukowe, ogłaszane corocznie przez Narodowe Centrum Nauki, mające na celu powołanie nowego zespołu badawczego prowadzącego badania naukowe o charakterze podstawowym. Kierownikiem projektu może zostać badacz, który uzyskał stopień naukowy doktora w okresie od 5 do 12 lat przed rokiem wystąpienia z wnioskiem.
Mój projekt zakłada między innymi opracowanie zmodyfikowanych genetycznie profagów oraz całkowicie syntetycznych, „wymyślonych” w laboratorium nowych wirusów bakteryjnych. Głównym celem jest zbadanie, jak określone zmiany genetyczne i tak zaprojektowane profagi wpływają na kondycję komórek bakterii i ich funkcjonowanie w środowisku.
Jako model badawczy do analizy roli (syntetycznych) profagów wybrałem bakterie pektynolityczne (Soft Rot Pectobacteriaceae – Pectobacterium spp. i Dickeya spp.). Bakterie te to patogeny roślin, w tym tych bardzo istotnych gospodarczo w Europie i na świecie. Bakterie te mogą przebywać w glebie, w wodzie, na różnych roślinach, być przenoszone przez owady, przeżywać na fragmentach roślin oraz w innych niszach środowiskowych. We wszystkich tych bardzo różnych środowiskach mogą napotykać na różne wirusy bakteryjne i być często infekowane, co może znacząco wpływać na ich adaptację do środowiska i zdolność wywoływania symptomów chorobowych na roślinach. Dlatego bakterie te stanowią tak dobry model badawczy do badania ich interakcji z wirusami.
Zrozumienie roli profagów w biologii bakterii pektynolitycznych może mieć istotne znaczenie dla rolnictwa i produkcji żywności. Wiedza na temat mechanizmów, które leżą u podstaw wirulencji i przystosowywania się tych bakterii, może przyczynić się do opracowania nowych strategii ochrony roślin przed chorobami. Co należy podkreślić: strategii naturalnych i bezpiecznych dla środowiska! W kontekście bakterii pektynolitycznych, profagi mogą być wykorzystane na przykład jako moduły do wprowadzania nowych funkcji lub cech do genomu bakterii. Dzięki zaawansowanym technikom inżynierii genetycznej możliwe jest zmodyfikowanie profagów poprzez dodawanie lub usuwanie ich genów odpowiedzialnych za kluczowe funkcje, takie jak wirulencja, odporność na stresy środowiskowe czy zdolność do konkurencji z innymi mikroorganizmami, oraz stworzenie nowych syntetycznych profagów. Z kolei w ramach projektowania syntetycznych genomów profagi mogą być wykorzystane do wprowadzenia do bakterii pektynolitycznych genów, które zwiększają ich zdolność do przetrwania i konkurencji w różnych warunkach środowiskowych.
Syntetyczne bakteriofagi mogą być zaprojektowane również tak, aby przenosiły specyficzne geny, które wprowadzone do bakterii prowadzą do ich śmierci. Dodatkowo możliwe jest wprowadzenie do genomów bakteriofagów genów kodujących enzymy degradujące ściany komórkowe bakterii, co zwiększa skuteczność infekcji i umożliwia bardziej efektywne zwalczanie patogenów. Syntetyczne bakteriofagi mogą być również wykorzystywane w precyzyjnych strategiach kontroli chorób, są wtedy aplikowane tylko na obszary dotknięte infekcją, minimalizując wpływ na inne (mikro)organizmy w ekosystemie.
Zastosowanie biologii syntetycznej do projektowania syntetycznych profagów i genomów bakteriofagów oferuje zatem szereg korzyści. Po pierwsze, pozwala na stworzenie wysoce specyficznych i specjalistycznych narzędzi do zwalczania patogenów, co minimalizuje ryzyko wpływu na inne mikroorganizmy w środowisku. Po drugie, syntetyczne bakteriofagi mogą być dostosowane do specyficznych warunków środowiskowych, co zwiększa ich skuteczność w różnych regionach geograficznych, typach upraw i warunkach pogodowych.
Ponadto możliwość precyzyjnego modyfikowania genomów bakterii i bakteriofagów otwiera drzwi do celowanej ochrony roślin, w której strategie kontroli są dostosowane do specyficznych potrzeb rolników. W erze katastrofy klimatycznej i rosnących zagrożeń związanych z chorobami roślin takie podejście stanie się kluczowym elementem zrównoważonego rolnictwa.
Mimo że biologia syntetyczna oferuje ogromne możliwości, jej zastosowanie w ochronie roślin wiąże się również z pewnymi wyzwaniami. Jednym z głównych problemów jest potencjalne ryzyko ekologiczne związane z wprowadzeniem sztucznie pozyskanych (modyfikowanych genetycznie) organizmów do środowiska. Dlatego konieczne jest przeprowadzenie szczegółowych badań nad bezpieczeństwem i wpływem takich organizmów na ekosystemy. Mój projekt zakłada zbadanie, jak takie zmodyfikowane i syntetyczne wirusy radzą sobie w środowisku i jak się w nim mogą rozprzestrzeniać.
Syntetyczne bakteriofagi reprezentują przyszłość w walce z infekcjami bakteryjnymi i chorobami roślin. Dzięki zaawansowanym technikom biologii syntetycznej możliwe jest projektowanie wirusów o niespotykanej dotąd specyficzności i skuteczności. W miarę postępu badań syntetyczne bakteriofagi mogą stać się kluczowym narzędziem w ochronie zdrowia i rolnictwa, otwierając nowe możliwości w zwalczaniu patogenów w sposób bezpieczny i ekologiczny.
Od początku kariery naukowej koncentruję się na badaniu interakcji bakterii patogennych dla roślin z ich środowiskiem. Moim głównym zainteresowaniem są mechanizmy molekularne i podstawy interakcji patogenów roślinnych – bakterii pektynolitycznych – ze środowiskiem. Obejmuje to interakcje z wirusami atakującymi bakterie (bakteriofagi lityczne i łagodne), innymi mikroorganizmami w środowisku (antagonistyczne bakterie, interakcje z nimi, wykorzystanie mikroorganizmów antagonistycznych w biologicznej ochronie roślin), a także interakcje z roślinami gospodarzami (proces kolonizacji i infekcji, rozpoznanie gospodarza na wczesnych etapach infekcji).
W ostatnich latach badania koncentrują się szczególnie na roli wirusów bakteryjnych (bakteriofagów) litycznych i łagodnych oraz ich białek w adaptacji i ewolucji bakterii pektynolitycznych w środowisku roślin. Badania te prowadzę wraz ze swoim zespołem dzięki finansowaniu w ramach projektu NCN SONATA Bis 10.
Mój zespół korzysta z szerokiego wachlarza technik badawczych, w tym mikrobiologii, biologii molekularnej, inżynierii genetycznej, badań mikroskopowych, biochemii oraz wykorzystania kultur tkankowych roślin.
W ramach swoich badań współpracuję z wieloma międzynarodowymi zespołami, m.in. z grupą prof. Stevena L. Lindowa z University of California-Berkeley, grupą dr. Erwana Gueguena z University of Lyon, prof. Celestina Mariani z Radboud University Nijmegen, a także z prof. Amy Charkowski z Colorado State University.
Prof. dr hab. Robert Czajkowski związany jest z Uniwersytetem Gdańskim, gdzie pracuje na Międzyuczelnianym Wydziale Biotechnologii UG i GUMed.